10月12日,中国国家药监局药品审评中心(CDE)网站最新公示,泽璟制药1类新药甲苯磺酸多纳非尼片上市申请拟纳入优先审评,本次申请的拟定适应症为——用于治疗晚期(无法手术或转移性)肝细胞癌。这不仅意味着多纳非尼有望在中国加速获批,也意味着泽璟制药将有望迎来首款获批上市的药品。

截图来源:CDE官网
多纳非尼是泽璟制药开发的口服多靶点、多激酶抑制剂类小分子抗肿瘤药物,属于1类新药。临床前药理学研究证实,该药既可抑制VEGFR、PDGFR等多种受体酪氨酸激酶的活性,也可直接抑制各种Raf激酶,并抑制下游的Raf/MEK/ERK信号传导通路,抑制肿瘤细胞增殖和肿瘤血管的形成,发挥多重抑制、多靶点阻断的抗肿瘤作用。

根据泽璟制药早前发布的新闻稿,本次新药上市申请主要是基于试验ZGDH3的结果。ZGDH3是一项开放、随机、平行对照、多中心的2/3期临床研究,由中国临床肿瘤学会(CSCO)副理事长秦叔逵教授主导,旨在探索多纳非尼片在晚期肝细胞癌患者一线治疗中的有效性与安全性。研究主要终点为总生存期(OS),次要终点包括无进展生存时间(PFS)、客观缓解率(ORR)、疾病控制率(DCR)、安全性及耐受性等指标。
试验结果显示,ZGDH3研究达到了预设的主要终点和统计学要求。在未接受过系统治疗的不可手术或转移性晚期肝细胞癌患者中,多纳非尼治疗组的中位总生存期(mOS)显著优于对照药物索拉非尼治疗组,达到统计学上差异显著性且具有临床意义的延长。此外,多纳非尼组在3级及以上不良事件发生率、与药物相关的导致停药或减量的不良事件发生率等方面显示出更优的安全性。
根据泽璟制药官网信息,在今年7月中国临床肿瘤学会发布的2020年版《原发性肝癌诊疗指南》中,多纳非尼已被列为晚期肝细胞癌一线治疗药物,并且是I级专家推荐和1A类证据。
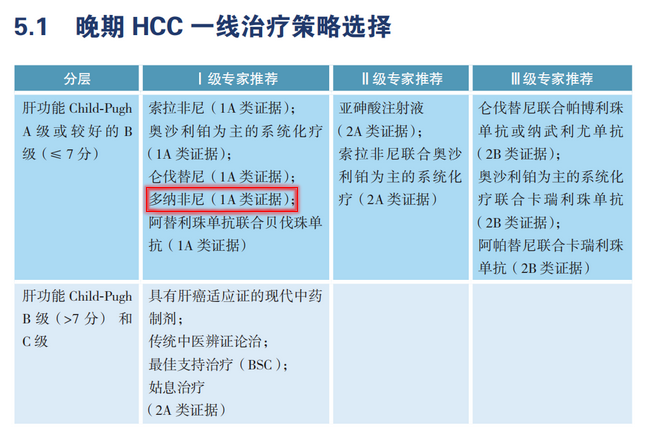
图片来源:泽璟制药官网
值得一提的是,ZGDH3研究结果摘要还成功入选了今年美国临床肿瘤学会(ASCO)年会的口头报告。据中国临床肿瘤学会介绍,这是十年来,由中国自主研发,且由中国学者主导的创新药物一线治疗晚期肝细胞癌的大型临床研究第一次在ASCO大会上向全世界公布成果和数据。
除了肝癌之外,目前,泽璟制药还在开展多纳非尼治疗晚期结直肠癌和甲状腺癌的关键性临床研究,同时也在积极推进多纳非尼联合PD-1/PD-L1单抗治疗多种肿瘤的新型研究。







