过去十年,双特异抗体的崛起就像是人类首次学会了如何建造精密的"战术桥梁":一端牢牢抓住潜伏在人体内的癌细胞,另一端则召唤并激活我们自身的免疫战士——T细胞,让它们能够跨越以往无法逾越的鸿沟,面对面与敌人进行决战。
然而,敌人向来不会坐以待毙,治疗过程中的癌细胞往往会展现出其狡猾本性,即改变表面抗原的表达模式,避开双抗的识别,并主动构建各种"防御工事"来抵抗免疫系统的攻击。
因此,科学家开始深入思考:能否设计出更加智能和坚固的"桥梁",让它不仅能够同时识别敌人的多种伪装,还能够招募不同类型的友军,形成更加全面和持久的包围攻势?
在此驱动下,三特异抗体应运而生,成为下一代免疫疗法研发的核心焦点。
从双抗到三抗
原则上来讲,三抗其实当属于21世纪才出现的全新技术类型。
2004年,三抗技术首次被Huang等人所提出,但受限于当时的技术瓶颈,未能如愿引起行业关注。
2010年后,随着免疫检查点抑制剂(如PD-1)和CAR-T疗法陆续获批,肿瘤免疫治疗技术逐渐趋于成熟,间接为多抗技术提供应用场景。
2022年,赛诺菲在《Nature》上连发多篇文章分享CD38/CD3/CD28三抗的研发进展,至此这一领域尝试正式进入大众视野。
2024年后,三抗研发明显加速,众多MNC与Biotech的研发热情逐渐由单抗、双抗向着三抗辐射。
而究其根本,之所三抗能在20余年里快速发展,一者是基础医学技术进步使然,二者也是双抗临床应用的局限性所致。
首先,如果把癌症治疗比作一场防御战,肿瘤细胞是城里的“伪装间谍”,而免疫细胞是我们的巡逻队。过去的双抗就类似于情报员,一手牵着白细胞特警队(T细胞),一手指着嫌疑目标(HER2肿瘤细胞),使T细胞更高效的杀灭肿瘤细胞。但问题是,抓捕过程中特警队会疲惫、会掉队,这就导致抗肿瘤效果往往是越来越差。
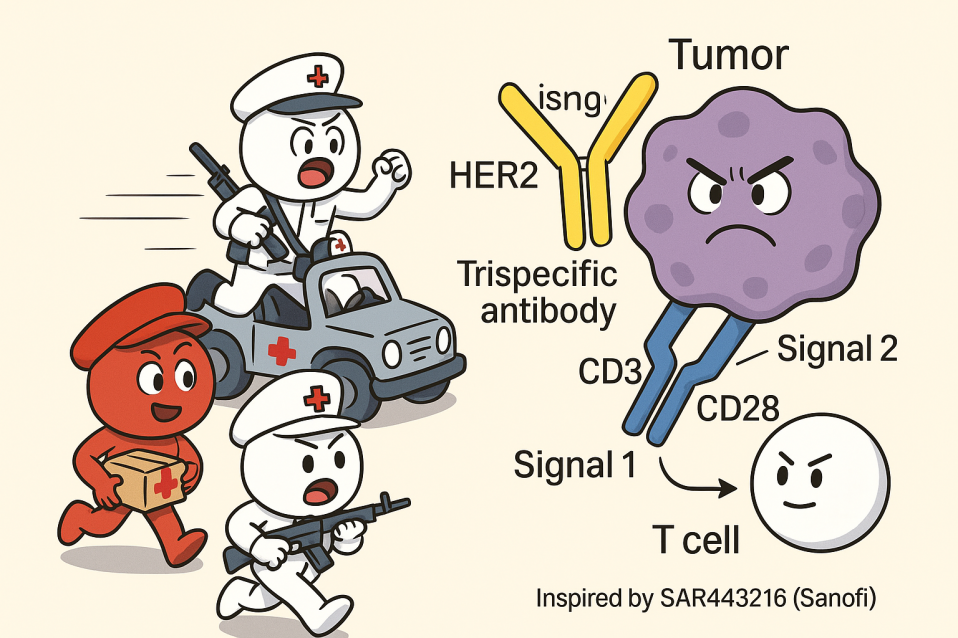
图1:三特异T细胞激活剂SAR443216(HER2×CD3×CD28)机理
图片来源:赛诺菲的Nature论文.doi: 10.1038/s41586-022-04439-0
而三特异性抗体则有所不同,其在双抗的基础上,继续与肿瘤细胞或免疫细胞表面的另一个靶点相结合,或桥接免疫细胞并阻断双信号通路等作用,更有利于将药物或免疫细胞重定向至肿瘤部位,增强结合特异性,提高靶向性,降低脱靶毒性,从而提升抗肿瘤能力。
以赛诺菲的SAR443216为例,其“三把钥匙”的独特机制,从本质上改变了抗肿瘤的整个故事线:
第一把钥匙(HER2)——红细胞搬运员送来位置地图,精准锁定目标大楼。
第二把钥匙(CD3)——白细胞特警队破门而入,开始清理现场。
第三把钥匙(CD28)——免疫司令部派来能量补给车(协同刺激信号),让特警队不但能打,还能在战斗中升级装备,形成“免疫记忆部队”。
更有意思的是,常被比喻成“支援兵”的 CD4+ T 细胞,在这个任务里竟然成了主攻队,直接干掉大部分敌人,同时呼叫支援部队释放“火力弹”(细胞因子),形成包围圈。这提示我们未来三抗设计需要更深入考虑免疫细胞群体间的协同作用,理解药物真实的作用机制,可能比设计药物本身更重要。
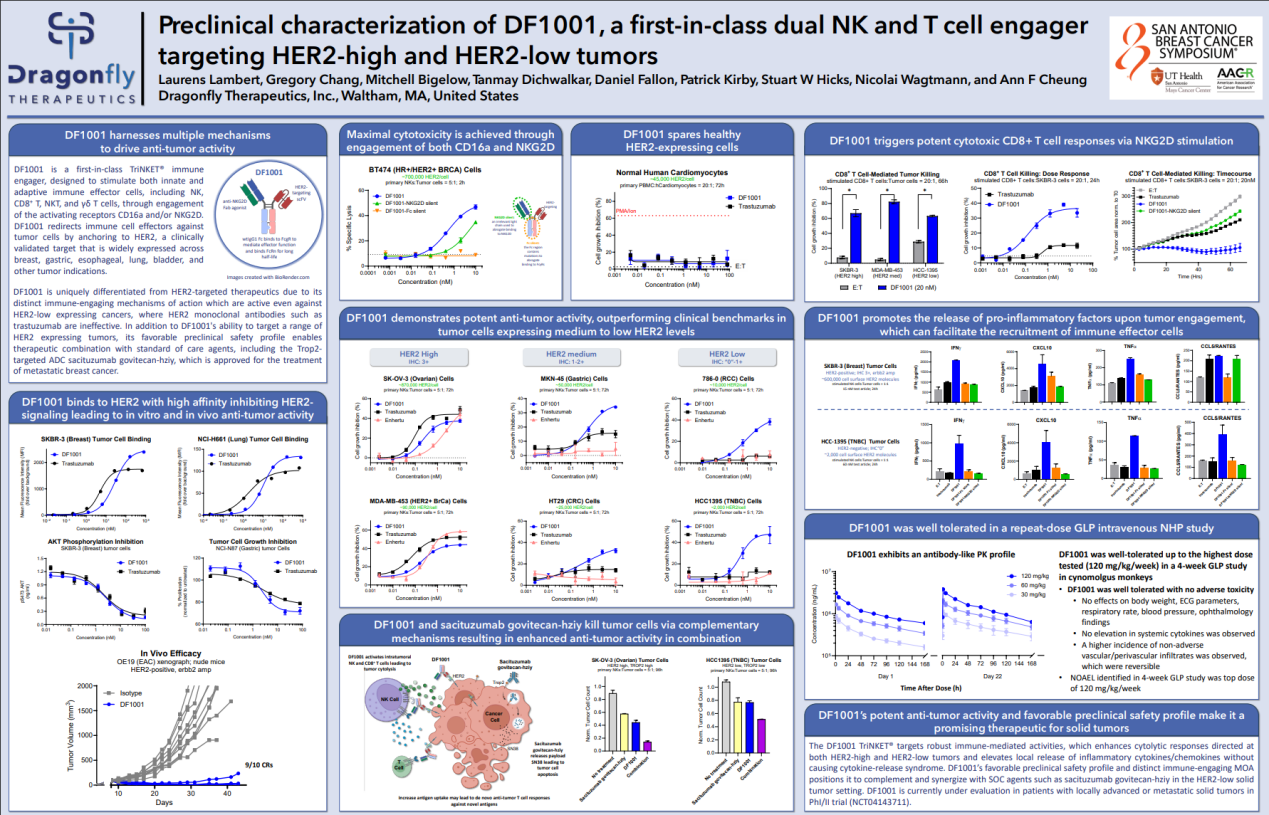
图2:DF1001的AACR学术海报
图片来源:Dragonfly官网
三抗成为“风口”的三大表现
1.全球管线数量集体爆发
近十年来,三特异性抗体(TsAb)从概念验证快速步入临床研究。早期的三特异性分子主要是“Trispecific Killer Engagers”(TriKE),用于在体外激活自然杀伤细胞,其核心是加入IL-15或其它细胞因子,项目停留在研究阶段。
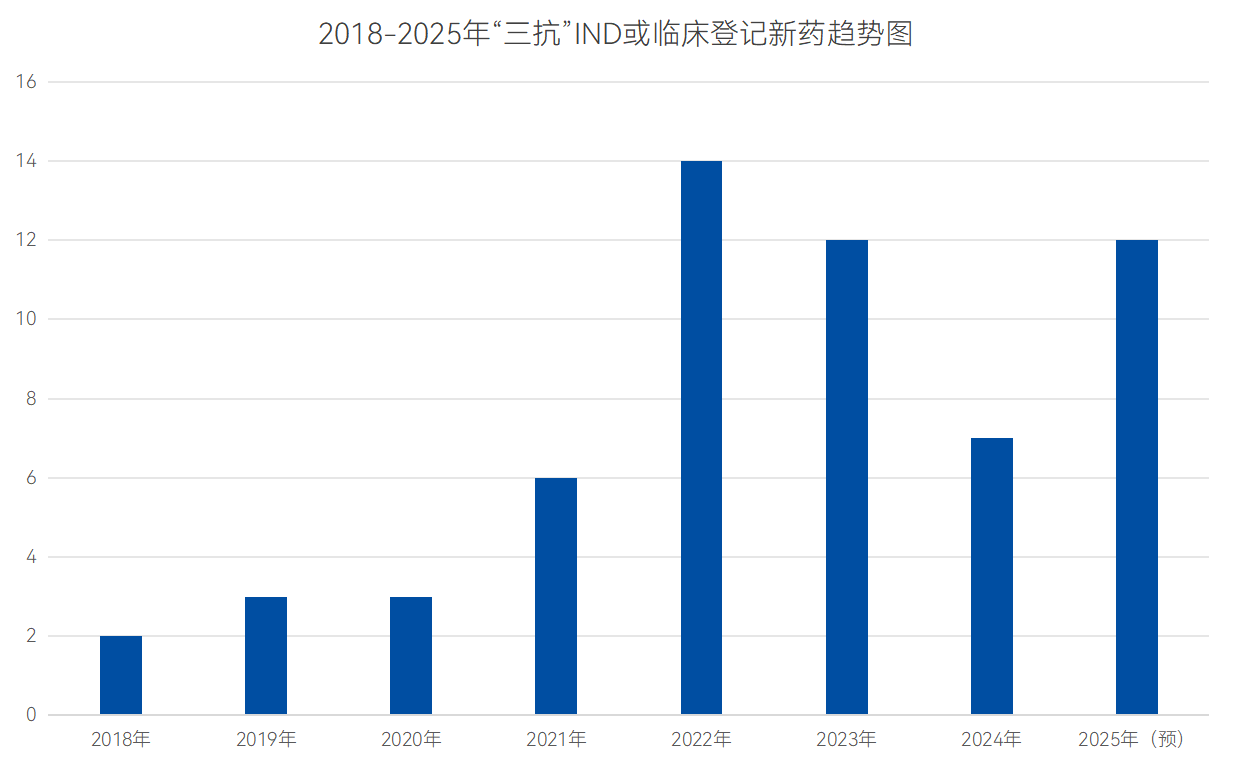
数据来源:药智数据
后来,随着工程化抗体平台成熟,首个真正的三特异性T细胞激活构建体(SAR442257)于2020年5月进入 I 期临床试验。截止目前,全球范围内已有超过50种三特异性抗体处于临床试验阶段,且数量逐年上涨。
全球部分在研进度居前的三抗管线
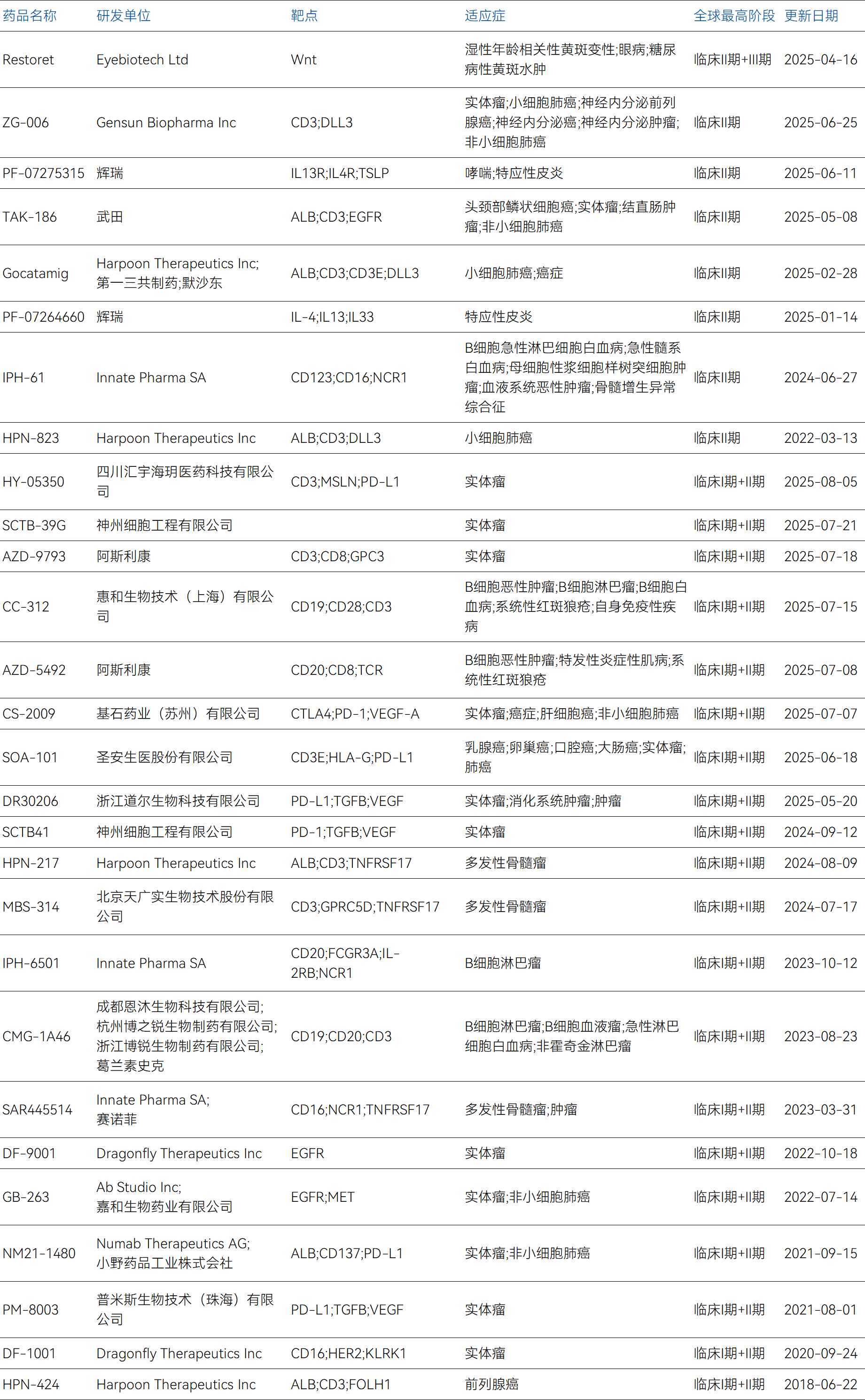
数据来源:药智数据
研发者构成方面,三抗领域内呈现出大型跨国制药公司与新兴生物技术公司共同活跃的格局。强生、赛诺菲、辉瑞、阿斯利康、葛兰素史克等跨国制药巨头凭借其雄厚的研发实力和丰富的临床经验,在技术平台建设和复杂项目推进方面发挥着引领作用。同时,以恒瑞医药、百济神州、康方生物、和铂医药、宏成生物为代表的国内生物技术公司也展现出强劲的创新活力,它们往往在特定的技术路径或适应症选择上具有独特的优势。
地域分布方面,当前临床开发的三特异性抗体主要集中在中国和美国,报告指出中美两国大约占据三抗全球70%左右的项目;欧洲(欧盟+英国)约占20%,其余项目由日本、澳大利亚和以色列等国承接,且中国在管线数量上的优势更加明显。
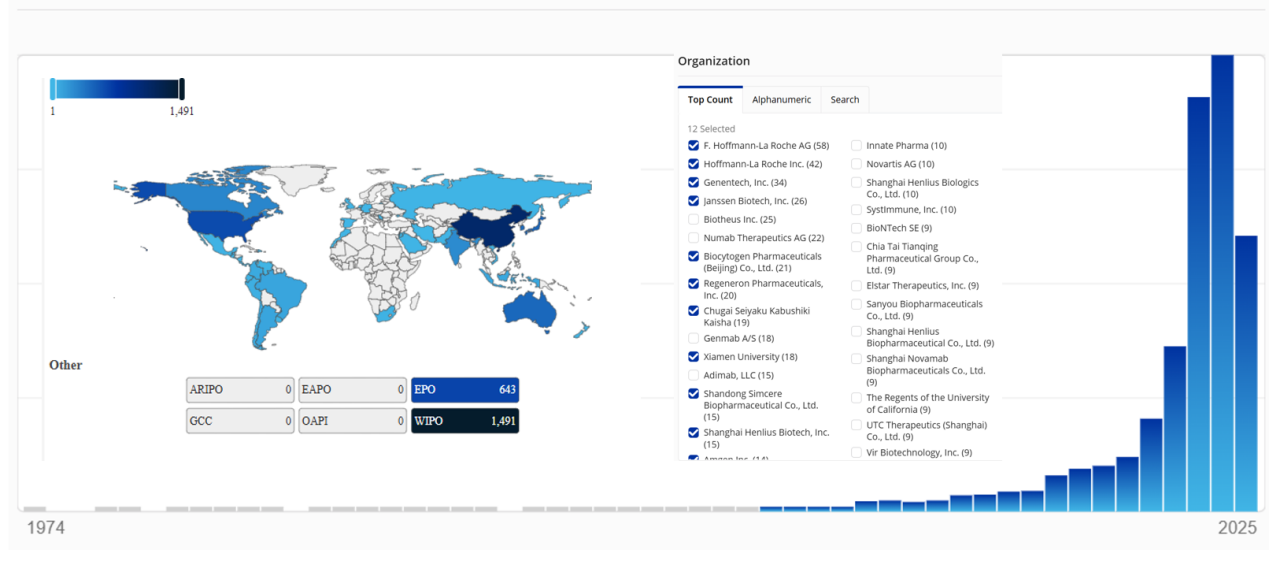
图3:多特异性抗体专利统计显示多特异性抗体专利近几年井喷式增长。
图源:笔者整理
至于中美领先的原因,前者主要得益于监管机构(NMPA)对创新抗体的快速审评,以及庞大的肿瘤患者基数提供临床试验市场;而后者则主要依赖于其成熟的创新药生态系统与完善的融资环境。
靶点选择策略方面,当前的三特异抗体设计主要围绕几个核心的靶点簇展开。其中最为主流的是以CD3为免疫效应细胞招募锚点,同时结合肿瘤特异性抗原如DLL3、GPRC5D、BCMA、EGFR、MSLN或CLDN18.2的组合设计。这种设计思路体现了将T细胞重定向与精准肿瘤识别相结合的治疗理念。
与此同时,免疫检查点的三联组合(如PD-1/PD-L1/CTLA-4/TIGIT/LAG3/VEGF的不同搭配)以及NK细胞相关的三联设计(如CD16×NCR1等组合)也在并行发展,反映出研发者们在免疫调节策略上的多元化探索。
适应症分布方面,肿瘤治疗占据了绝对主导地位,这与三特异抗体在免疫肿瘤学领域的技术优势密切相关。血液肿瘤和实体瘤成为两大核心应用场景,前者由于其相对均质的抗原表达和免疫微环境特点,往往成为新技术的首选验证领域。值得注意的是,三特异抗体的应用范围正在向肿瘤之外的领域扩展,包括炎症性疾病、自身免疫疾病、感染性疾病(如HIV-1、SARS-CoV-2)以及眼科疾病,这种外延发展预示着该技术平台具有更广阔的治疗潜力。
技术构型方面,多样化是当前三特异抗体发展的另一个显著特征。传统的IgG×Fab×scFv格式之外,新兴的设计如sdAb-scFv-sdAb、(Fab+Fab-Fab)-Fc等形式正在增多。特别值得关注的是条件性激活格式的兴起,包括TRACTr、ProTriTAC以及基于掩蔽肽的设计等,这些创新格式旨在提高治疗的精准性和安全性,通过在特定的肿瘤微环境条件下才激活抗体功能,从而减少对正常组织的影响。
2.MNC交易频繁
近几年以来,围绕三抗的资本盛宴已然开席,三抗相关交易持续升温。可以看到,下场的MNC越来越多。尽管这些管线仍处于早期阶段,但也向外界传递着一个明确的信号,那就是,三抗已经彻底火起来了。
2025年1月,艾伯维与先声再明达成GPRC5D/BCMA/CD3三抗SIM0500的10.55亿美元合作,艾伯维在血液瘤领域的又一次出手。
2025年7月,艾伯维斥资7亿美元预付款,总金额近20亿美元引进IGI Therapeutics SA(IGI)公司的三特异性抗体新药ISB 2001,获得在北美、欧洲、日本和大中华区开发、制造和商业化的独家权利。
2024年1月,默沙东以6.8亿美元收购Harpoon Therapeutics,获得DLL3/CD3/Albumin三抗HPN328(MK-6070)等一系列TCE产品。默沙东目前正在进行MK-6070用于小细胞肺癌的临床Ⅱ期研究。
2024年10月,GSK以3亿美元的首付款、5.5亿美元的开发和商业化里程碑付款,从恩沐生物引进CD3/CD19/CD20三抗CMG1A46。
2024年3月,吉利德以5600万美元预付款及最高15亿美元里程碑付款,与Merus达成合作,联手开发新型肿瘤相关抗原(TAA)的三抗。
3.MNC自研积极
当然,除了依靠BD模式快速扩充三抗在研管线外,MNC通常情况下也会不遗余力的推进“自研三抗”的落地。
部分MNC原研的三特异性抗体管线
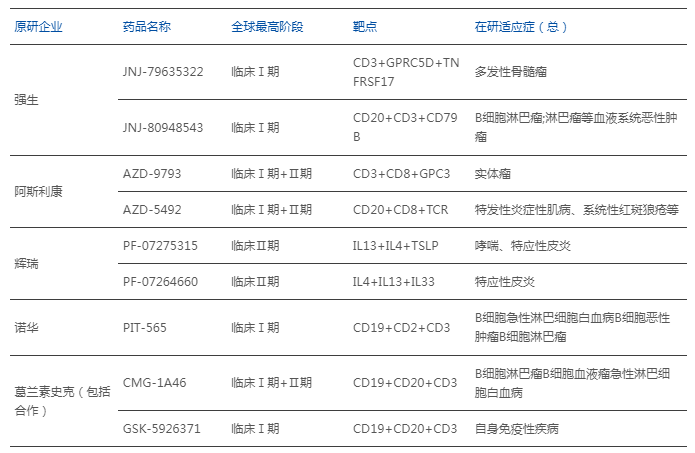
数据来源:药智数据
强生的JNJ-5322,在2025年ASCO年会上首次披露相关临床数据,以在未接受过BCMA/GPRC5D治疗的RRMM患者中近100%的ORR数值,技惊四座,且在三药耐药的患者中,ORR高达86%,疗效堪比CAR-T,有望成为下一代MM治疗领域的有力竞争者。
阿斯利康开发的AZD5492是全球首款CD20/TCR/CD8三特异性抗体,该药用于复发性或难治性B细胞恶性肿瘤和系统性红斑狼疮、特发性炎症性肌病,均已进入临床研究。阿斯利康另一款三抗药物AZD9793(靶向GPC3/TCR/CD8)也已启动1期临床试验,拟用于多种实体瘤。
辉瑞:已在炎症免疫领域推进两款三特异抗体,PF-07275315(IL-4/IL-13/TSLP)与PF-07264660(IL-4/IL-13/IL-33),均用于特应性皮炎,处于 II 期临床;策略为“一针阻断多条 II 型炎症通路”,试图在 Dupilumab 之外进一步降低复燃与难治人群负担。
诺华:PIT565(CD19×CD3×CD2)为First-in-Class 三特 T 细胞连接器,依托 CD2 共刺激以缓解 T 细胞衰竭,用于复发/难治 B 细胞恶性肿瘤,I 期临床进行中,已在 ASH 2023 发布研究设计与早期安全/药理学信息。
GSK:GSK-5926371(CD19×CD20×CD3)定位于自身免疫性疾病,I 期管线已在官方管线报告披露;路径为“低亲和 CD3 牵引 + B 细胞双靶去Plet化”,意在提升效力同时控制安全窗。GSK简评:三家路线各有侧重——辉瑞押注细胞因子轴并联(皮肤免疫),诺华与GSK侧重B细胞病理(血液/自身免疫)。与贵文“交易扩张并行自研落地”的判断一致,且进一步说明三抗正由平台化概念走向适应症定制化工程。
三抗的挑战与应对策略
从技术工程的角度来审视,我们正在见证多个独立的创新领域的深度融合。条件性激活和掩蔽肽触发机制让抗体能够像智能导弹一样,只在到达预定目标区域后才"解除保险",而位点特异偶联技术则确保了载荷药物能够精确地连接在抗体的指定位置上。
这种精密控制不仅能够显著扩大治疗的安全窗口,还为临床治疗提供了更多的治疗策略选择,无论是采用序贯给药的渐进式攻击,还是选择同步联合的饱和式打击。
当然,我们也必须诚实地面对这种技术融合带来的新挑战。如果把传统单抗比作制造一把简单而可靠的工具,那么三特异抗体就像是要制造一台能够同时执行三种不同任务的精密设备。这种复杂性的提升带来了前所未有的技术挑战。
首先是分子工程复杂性这一根本性挑战,三特异抗体需要三条或更多蛋白链精确配对组装,就像搭建一座需要多种零件完美契合的复杂建筑。与传统抗体的对称结构不同,这种不对称分子极易产生错误配对,导致大量废品。更麻烦的是,正确组装的产物也常常表现出高度异质性,容易聚集,在治疗浓度下黏度显著增加,让传统制剂技术捉襟见肘。
其次是安全性风险的多重叠加,三特异抗体设计的初衷是强烈激活免疫细胞,但这把双刃剑在杀伤肿瘤的同时也可能引发危险的细胞因子风暴,当与ADC联用时,免疫激活的毒性与化疗载荷的毒性相遇,就像两股不同的风暴汇聚,可能产生比单独出现时更严重的后果。
之后是来自药代动力学特性的不理想,大多数三特异抗体半衰期较短,需要频繁给药或持续输注。同时,复杂的分子结构和高疏水性表面让制剂配方和给药方式都面临新的技术难题。
最后是适应症选择的现实局限。虽然在血液肿瘤中表现出色,但三特异抗体在实体瘤领域仍然举步维艰。实体瘤缺乏理想的肿瘤特异抗原,存在显著异质性,加上免疫抑制微环境的阻碍,让理论优势难以转化为临床价值。
面对这些系统性挑战,全球制药企业正在多个维度上展开创新攻关,形成了相互关联而又各有侧重的解决方案体系。
针对分子工程复杂性,各大企业主要通过先进的蛋白质工程技术来解决。比如赛诺菲的BEAT平台、恒瑞与Ichnos的MATCH技术、广泛应用的CrossMAb技术等,都是为了确保多链分子的正确配对。这些平台就像为复杂设备设计的精密装配线,通过特殊的"锁扣"机制大大提高产物纯度。定点偶联技术更是将精确控制推向新高度,让载荷药物能够精准连接到指定位置。
针对安全性挑战,条件激活与掩蔽策略成为突破口。默沙东的ProTriTAC、Takeda的TRACTr、国内的COBRA平台等,都采用在关键结合域前端添加可酶切掩蔽肽的策略。这种设计让抗体像智能导弹一样,只在到达肿瘤微环境后才"解除保险"。TwoGATE™技术则更加巧妙,将CD3结合位点分割为两部分,只有当两个抗体同时结合同一肿瘤细胞时才形成完整激活信号,实现了前所未有的精准控制。
针对药代动力学不理想,企业通过制剂技术优化,筛选新型辅料、优化缓冲体系、降低分子疏水性等手段解决高黏度问题。透明质酸酶共制剂技术为皮下给药开辟新途径,蛋白结合域或Fc工程改造延长半衰期,一些企业还在探索延释剂型开发,临床策略的精细化管理已成为确保安全有效应用的关键。
当然,也正是基于对挑战的深刻认识,业界在临床开发策略上体现出应有的审慎智慧。分期序贯开发让研究者充分评估风险收益,低剂量起始确保患者安全第一,基于生物标志物分层的精准医学方法让治疗真正因人而异。这种渐进式概念验证策略虽然可能延长开发周期,但为最终成功提供更坚实基础。
通过这种系统性的挑战分析和解决方案梳理,我们可以看到三特异抗体正在从"技术可行"向"临床实用"转变。跨国企业凭借强大平台在复杂工程和安全管理方面引领,国内公司在独特靶点组合和快速推进方面展现活力。随着新技术平台成熟和人工智能深度应用,三特异抗体有望逐步突破当前瓶颈,在更广泛的癌症治疗中发挥价值。
三抗的未来方向
随着三特异抗体技术日趋成熟,三特异性抗体的未来发展方向成为企业首要考虑的问题之一。当前研究重点正从基础结构优化转向临床应用场景的深度挖掘,例如通过多靶点协同机制实现对复杂疾病(如肿瘤微环境调控、自身免疫性疾病)的精准干预。
而在技术路径上,行业主要呈现三大趋势:
技术迭代:很明显,三抗绝非创新疗法终点,未来一方面有望向着四特异性抗体演进,整合更多免疫调节信号(如IL-15、NKG2D),增强抗肿瘤效果及免疫应答持久性;另一方面则可能通过结构创新(如前药设计、遮蔽肽技术)降低细胞因子释放综合征(CRS)等毒性风险,并优化生产工艺以解决多靶点抗体的复杂性难题。
适应症扩展:就现阶段三抗适应症分布而言,血液肿瘤与实体瘤是最主要的适应症范围,但值得注意的是,三特异抗体的应用范围正在向肿瘤之外的领域扩展,未来有望辐射至更多炎症性疾病、自身免疫疾病、感染性疾病(如HIV-1、SARS-CoV-2)以及眼科疾病,这种外延发展预示着该技术平台具有更广阔的治疗潜力。
联合疗法:与CAR-T、ADC(抗体偶联药物)、化疗等联用,克服单药疗效瓶颈,例如赛诺菲探索三抗+化疗组合以提升耐药性肿瘤的治疗效果。
其中,联合疗法是目前三抗最有希望率先落地的方向之一,也是绝大多数药企紧密推进的内容方向,尤其是“三抗+ADC”。
对于该联合方案,三特异抗体就好比一位经验丰富的侦察兵,它的任务是精准识别敌人的多个特征标志,同时呼叫友军支援。而ADC技术则像是携带精确制导弹药的轰炸机,专门负责对那些隐藏较深或防御较强的目标进行直接打击。当这两种力量协同作战时,就能够应对肿瘤细胞的各种狡猾策略,无论是抗原表达的变化、免疫微环境的"冷淡",还是传统治疗方法难以触及的顽固病灶。
小结
当我们回望双特异抗体十年来从实验室走向临床的征程,会发现这场变革的真正意义远超技术本身——它重新定义了我们构建分子"桥梁"的思维方式。双特异抗体教会了我们如何精准连接免疫细胞与肿瘤细胞,但面对癌症的狡猾多变,我们很快意识到:仅仅复制成功是不够的,我们需要让这座桥梁变得更加智能和坚固。三特异抗体的兴起标志着整个领域正在经历一场深刻的转变——从早期的"概念热潮"转向"证据驱动的精细竞赛"。
这种转变揭示了一个重要规律:当技术的门槛被普遍跨越后,真正的差异化就不再是"能做什么",而是"能做得多好"。成功的三特异抗体需要在靶点组合、信号工程和给药策略三个维度上实现系统性卓越,而非简单的分子复杂度堆砌。更引人深思的是产业生态的同步升级。如果说早期抗体开发还带有"手工作坊"的色彩,那么今天的三特异抗体已经步入"精密制造"时代。
以博腾为代表的CDMO企业正从单纯的"代工厂"蜕变为"技术合作伙伴",这种角色转换提醒我们:在高度复杂的创新领域,成功需要整个生态系统的协同进化。最具前瞻性的开发者们正在践行"阶梯式技术演进"的智慧——先通过成熟的三特异技术建立安全基础,再探索与ADC等先进技术的整合,始终以生物标志物为精准医学的指南针。这种渐进式创新体现了对技术发展规律的深刻理解:真正的突破往往不是颠覆性的跳跃,而是在扎实基础上的持续优化与智慧整合。
无论技术如何演进,竞争如何激烈,有一点永远不应改变:一切创新的终极目标都是为患者创造更好的治疗方案。当我们能够将精巧的分子工程与深刻的患者需求洞察相结合时,才能创造出真正具有持久价值的医疗突破。这或许就是从双特异到三特异这场技术进化最值得铭记的启示。







